Forschung
AG Bioorganische ChemiePeptide sind durch ihre zahlreichen und vielseitigen Funktionen in der Natur bekannt, wo sie beispielsweise als Hormone (z.B. Oxytocin) und Entzündungshemmer (z.B. Melittin) agieren können oder auch als Toxine (z.B. a-Amanitin) produziert werden [1]. In den letzten Jahrzehnten haben sie darüber hinaus aufgrund ihrer Vielseitigkeit und Spezifizität auch in der chemischen, pharmazeutischen und kosmetischen Industrie an Bedeutung gewonnen, sodass heutzutage intensiv an neuen, natürlichen und synthetischen Peptiden geforscht wird [2]. In der bioorganischen, biochemischen und molekularbiologischen Forschung stellen Peptide wesentliche Werkzeuge dar, um wissenschaftliche Fragestellungen zu lösen.
[1] Daffre, S., Bulte, P., Spisni, A., Ehret-Sabatier, L., Rodrigues, E. G., Travassos, L. R. (2008) Bioactive natural peptides. Stud. Nat. Prod. Chem. 35, 597-691.
[2] Muttenthaler, M., King, G. F., Adams, D. J., Alewood, P. F. (2021) Trends in peptide drug discovery. Nat. Rev. 20, 309-325.
Häm/Thrombose-Forschung
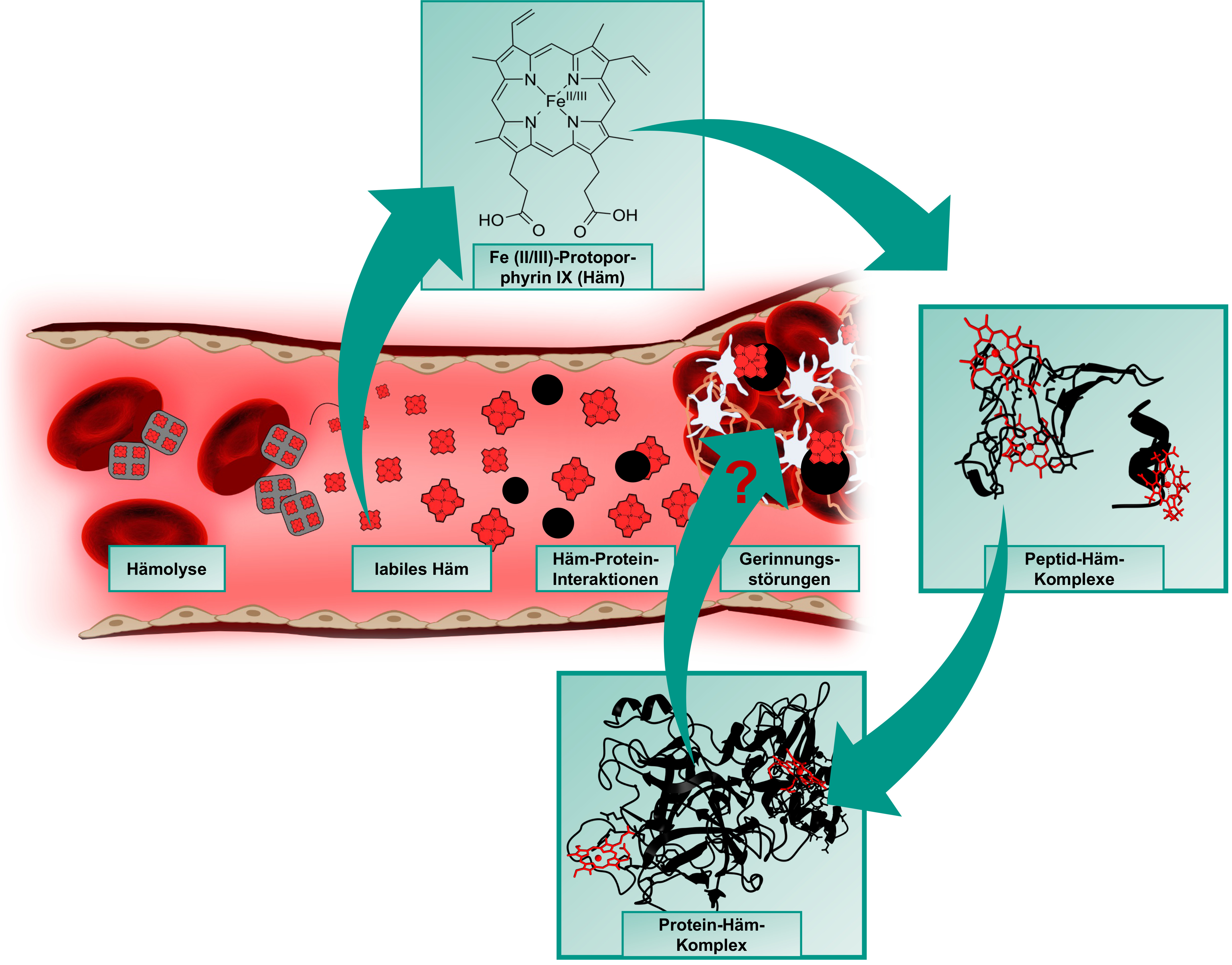
Die Komplexverbindung Häm (Eisen(II/III)-Protoporphyrin IX) ist vorrangig durch seine Rolle als Sauerstoff-bindende, prosthetische Gruppe des Hämoglobins bekannt und zirkuliert als solches in Mengen von insgesamt ~25 Trilliarden Molekülen in den Erythrozyten im Blut des menschlichen Körpers. Im Zuge von intravaskulärer Hämolyse, wie sie bei Erkrankungen, wie der Sichelzellanämie, oder als Folge von Transfusionen auftreten kann, kommt es zu einer frühzeitigen Zerstörung der Erythrozyten und so zu einer massiven Freisetzung von Hämoglobin und infolgedessen zu der Akkumulation von labilem Häm im Blut. In dieser Form kann Häm transient an Proteine binden und deren Stabilität und/oder Funktion beeinflussen [1-3].
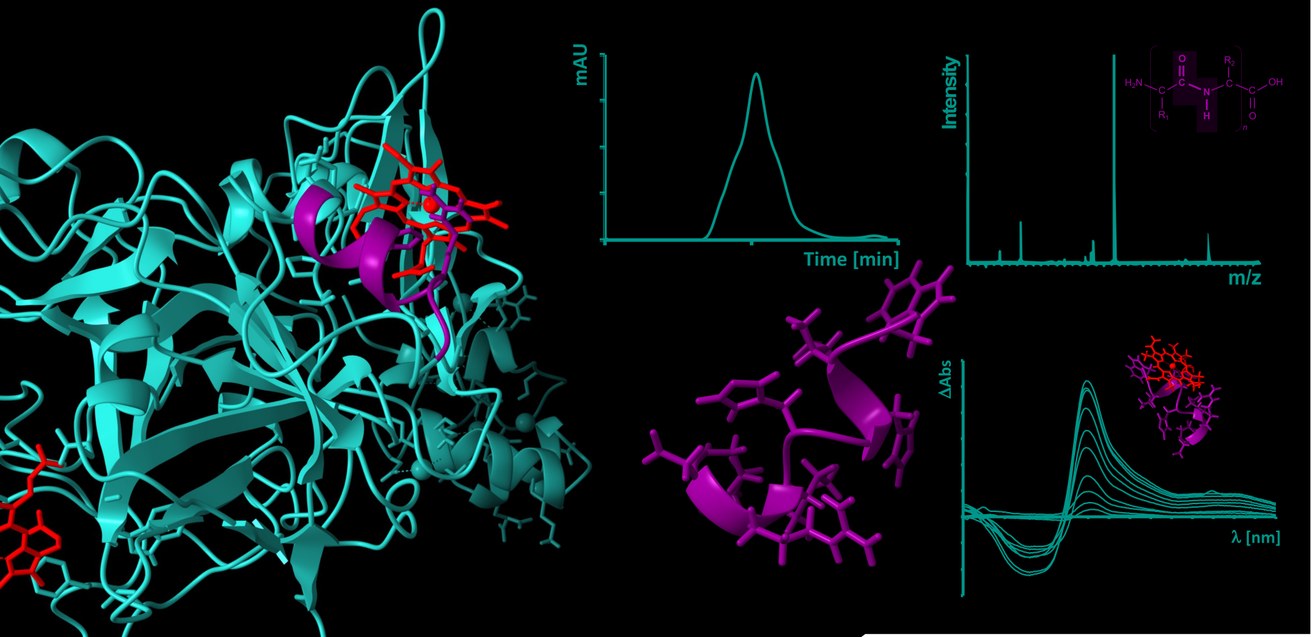
Eine der Hauptkomplikationen von hämolytischen Ereignissen stellen venöse prothrombotische Gerinnungsstörungen, wie tiefe Venenthrombosen oder Lungenembolismus, dar. Deren molekulare Grundlage ist bis heute nicht vollständig aufgeklärt, jedoch gibt es Hinweise darauf, dass auch hierbei labiles Häm und dessen Interaktion mit an diesen Prozessen beteiligten Plasmaproteinen eine Rolle spielt [4,5]. Eben diese Häm-Protein-Interaktionen sind sowohl auf molekularem Level als auch im Kontext ihrer (patho-)physiologischen Relevanz weitesgehend unerforscht. Wie zuvor bereits mit dem endogenen Gerinnungsinhibitor APC und dem Gerinnungsfaktor VIII gezeigt [6,7], zielen wir mit unseren DFG- und GTH-geförderten Projekten (vgl. Projekte unten) nun darauf ab, das Gerinnungssystem als Häm-reguliertes System auf der Ebene der potentiellen Häm-Protein-Interaktionen unter Verwendung von Protein-abgeleiteten Peptiden zu untersuchen und zu charakterisieren. Erst kürzlich konnten wir in diesem Kontext das gerinnungshememmende Protein Z als Häm-reguliertes Protein charakterisieren [8].
[1] Soares, M. P., Bozza, M. T. (2016) Red alert: Heme is an alarmin. Curr. Opin. Immunol. 38, 94-100.
[2] Roumenina, L. T., Rayes, J., Lacroix-Desmazes, S., Dimitrov, J. D. (2016) Heme: Modulator of plasma systems in hemolytic diseases. Trends Mol. Med. 22(3), 200-213.
[3] Kühl, T., Imhof, D. (2013) Regulatory FeII/III heme: The reconstruction of a molecule's biography. ChemBioChem 15(14), 2024-2035.
[4] Hopp, M.-T., Imhof, D. (2021) Linking labile heme with thrombosis. J. Clin. Med. 10(3), 427.
[5] Mubeen, S., Domingo-Fernandez, D., Díaz del Ser, S., Solanki, D., Kodamullil, A. T., Hofmann-Apitius, M., Hopp, M.-T., Imhof, D. (2022) Exploring the complex network of heme-triggered effects on the blood coagulation system. J. Clin. Med. 11(19), 5975.
[6] Hopp, M.-T., Alhanafi, N., Paul George, A. A., Hamedani, N. S., Biswas, A., Oldenburg, J., Pötzsch, B., Imhof, D. (2021) Molecular insights and functional consequences of the interaction of heme with activated protein C. Antioxid. Redox Signal. 34(1), 32-48.
[7] Hopp, M.-T., Ugurlar, D., Pezeshkpoor, B., Biswas, A., Ramoji, A., Neugebauer, U., Oldenburg, J., Imhof, D. (2024) In-depth structure-function profiling of the complex formation between clotting factor VIII and heme. Thromb. Res. 237, 184-195.
[8] Lindemann, P., Hopp, M.-T. (2026) Human protein Z as the second known heme-binding protein from the endogenous blood coagulation inhibitor system. ChemBioChem, doi: 10.1002/cbic.202500636.
Amphibiensekret-Forschung
Naturstoffe, und insbesondere Peptide, stellen äußerst attraktive Kandidaten für die moderne Wirkstoffforschung und -entwicklung dar [1]. Zu den bekanntesten Peptidtherapeutika zählen unter anderem das Analgetikum Ziconotid, das von einem Peptid abgeleitet wurde, welches ursprünglich aus dem Gift der Kegelschneckeisoliert wurde, sowie Antidiabetika, die auf dem Peptid Exendin-4 basieren, das erstmals im Speichel des Gila-Krustenechse identifiziert wurde [2–4]. In diesem Zusammenhang haben Amphibiensekrete in den vergangenen Jahrzehnten zunehmend wissenschaftliche Aufmerksamkeit erlangt. Diese Sekrete erfüllen sowohl Schutz- als auch Abwehrfunktionen und enthalten eine Vielzahl biologisch aktiver Moleküle, darunter Toxine, biogene Amine, Alkaloide sowie bioaktive Peptide [1,4,5]. Während bereits zahlreiche Hautpeptide aus Fröschen und Kröten isoliert und umfassend untersucht wurden, sind diejenigen aus Salamandern und Molchen bislang vergleichsweise wenig erforscht [5,6]. Die bisher aus Hautsekreten von Salamandern und Molchen identifizierten Peptide zeigen jedoch ein breites Spektrum vielversprechender biologischer Aktivitäten, darunter antimikrobielle, antioxidative, wundheilungsfördernde, entzündungshemmende sowie myotrope Effekte [6,7]. Aufbauend auf diesen Erkenntnissen zielt unser Projekt darauf ab, die bislang weitgehend unterschätzten Sekrete der Schwanzlurche (Caudata) näher zu untersuchen, mit besonderem Fokus auf Peptide aus Salamandern, Molchen sowie generell aus heimischen Amphibienarten [4]. Zu diesem Zweck führen wir Peptidsynthesen, strukturelle und funktionelle Charakterisierungen sowie systematische Untersuchungen verschiedener Bioaktivitäten durch. Diese experimentellen Ansätze werden durch in-silico-Analysen ergänzt, um mechanistische Einblicke zu gewinnen und beobachtete biologische Effekte, beispielsweise antimikrobielle Aktivität, besser zu verstehen [7].
[1] Muttenthaler, M., King, G. F., Adams, D. J., Alewood, P. F. (2021) Trends in peptide drug discovery. Nat. Rev. Drug. Discov. 20, 309-325.
[2] Lyseng-Williamson, K. A., Perry, C. (2006) Ziconotide. CNS Drugs. 20, 331-338.
[3] Yap, M. K. K., Misuan, N. (2018) Exendin-4 from Heloderma suspectum venom: From discovery to its latest application as type II diabetes combatant. Basic Clin. Pharmacol. Toxicol. 124, 513-527.
[4] Hopp, M.-T. (2026) Wirkstoffreich aber unterschätzt: Heimische Amphibien als Quelle bioaktiver Peptide. Chem. unserer Zeit 70025.
[5] Kröner, L., Lötters, S., Hopp, M.-T. (2024) Insights into caudate amphibian skin secretions wit a focus on the chemistry and bioactivity of derived peptides. Biol. Chem. 405, 641-660.
[6] Xu, X., Lai, R. (2015) The Chemistry and Biological Activities of Peptide from Amphibian Skin Secretions. Chem. Rev. 115, 1760-1846.
[7] Kröner, L., Meier, J., Hopp, M.-T. (2026) Bioactive Peptide from Caudate Amphibians: Synthesis and Assessment of Antioxidant and Antimicrobial Activities. J. Nat. Prod. 10.1021/acs.jnatprod.5c01604